-
新闻
脂肪干细胞的3D培养和外泌体收获研究
发布日期:2024-12-02
人脂肪组织来源的间充质干细胞(adipose-derived stem cells,ADSCs)是间充质干细胞的主要来源之一,其被认为是干细胞治疗和再生医学领域极有潜力的工具。ADSCs可分化为外胚层、中胚层和内胚层三个谱系的细胞,可通过释放外泌体(Exosomes)、生长因子等成分来调节细胞微环境,具有抗凋亡、抗炎、促进血管生成、调节免疫功能、抗瘢痕形成等作用。 脂肪干细胞外泌体(ADSCs-EXOs)是ADSCs向细胞外分泌的小囊泡,可以运输多种细胞成分并与靶细胞融合,介导局部和系统性的细胞间通讯,从而调节受体细胞生物学行为[1]。ADSCs-EXOs具有性质稳定、便于管理和运输、不含活细胞、生物学功能不随时间延长而衰减、低抗原性等优点。 研究表明ADSCs-EXOs在多种疾病中显示出较高的诊断价值和治疗潜力,例如糖尿病、伤口愈合、神经退行性疾病、心血管疾病、骨再生等方面,尤其是在伤口愈合中的临床应用价值很高,且作用机制已清晰揭示[2](图1)。

图1. 脂肪间充质干细胞外泌体在伤口愈合的临床应用及机制[2]
研究表明,不同来源的间充质干细胞的外泌体产量和颗粒大小都有差异。脐带间充质干细胞(UCMSCs)每个细胞产生的外泌体是来自骨髓(p=0.0063)或脂肪组织(p=0.006)的间充质干细胞的四倍。来UCMSCs的外泌体也比来自骨髓(140+18nm; p=116.9)和脂肪组织(0+01nm; p=105.12)间充质干细胞的外泌体大(0±0004nm) [3] (图2)。因此如何获得足够量的ADSCs-EXOs成为其临床应用的一个挑战。
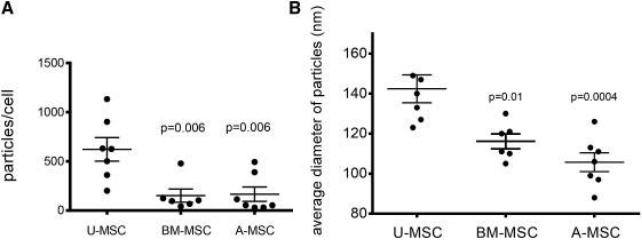
图2. 不同来源间充质干细胞外泌体的产量和粒径比较[3]
同腾新创自主研发的CEL-G® Culture Ad60系列固定床生物反应器(Ad60 FBR),适用于大规模细胞培养、cGMP级病毒生产及外泌体收获,独特的技术为细胞生长提供低剪切力的3D培养环境。前期我们已报道采用Ad60 FBR实现了UCMSCs的连续培养和外泌体收获(图3),在2平米面积的固定床上培养UCMSCs,外泌体颗粒浓度可达到3×1011 Particles/mL,外泌体总产量可达到1.1×1015 Particles。

图3. CEL-G® Culture Ad60 系列固定床生物反应器
本次实验通过研究ADSCs在2D培养条件下及Ad60 FBR中的生长情况,探索ADSCs的2D培养情况及3D培养工艺和ADSCs-EXOs的收获产量。
为了了解不同培养基对ADSCs生长情况的差异,我们使用不同品牌的MSC无血清培养基对ADSCs进行生长曲线测试,分别使用同腾新创自主开发的CEL-G® Culture MSC Basal SFM间充质干细胞无血清基础培养基、CEL-G® Culture MSC ExoPro SFM间充质干细胞外泌体生产无血清培养基、国产品牌-1和国产品牌-2。使用不同品牌的完全培养基分别将ADSCs接种于6孔板中,并于接种后每隔24h进行消化计数,检测结果如图4所示。
结果显示,MSC ExoPro SFM及MSC Basal SFM两款培养基培养的ADSCs较另两款培养基细胞生长更快。
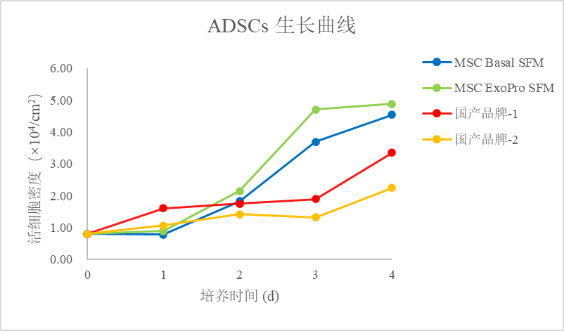
图4. ADSCs在不同培养基中的生长曲线测试
我们通过将ADSCs接种于6孔板中进行2D条件下培养,使用不同品牌的完全培养基进行培养,待细胞生长至90%左右时更换为不含营养添加物的培养基继续培养4天,检测上清中外泌体含量,检测结果如图5所示。结果显示,使用MSC ExoPro SFM及MSC Basal SFM进行2D培养,外泌体单位浓度可分别达28×109particles/mL和22×109particles/mL,相比国内同类培养基,外泌体产量提高了75%及70%。
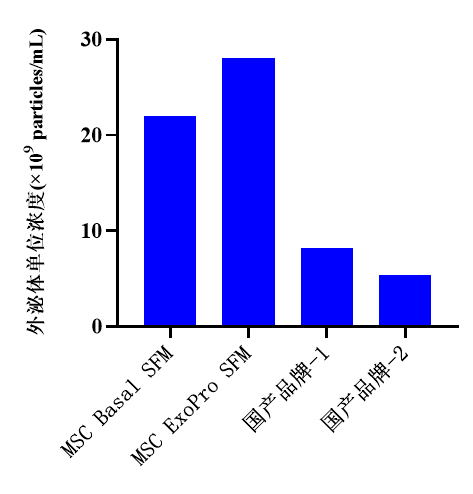
图5. ADSCs在2D 条件下外泌体产出情况
为了进一步了解ADSCs的生长情况及外泌体产出情况,我们将ADSCs使用Ad60 FBR FB-2(2平米固定床)进行3D培养。培养总周期为14天,每天取上清检测游离细胞及生化指标(图6),每天取取样条进行活细胞荧光染色观察(图7)。在外泌体收获阶段,分别于Day6、Day8、Day10、Day12及Day14进行细胞上清的全收获,每批次收获外泌体进行NTA检测,产量数据如图8所示。
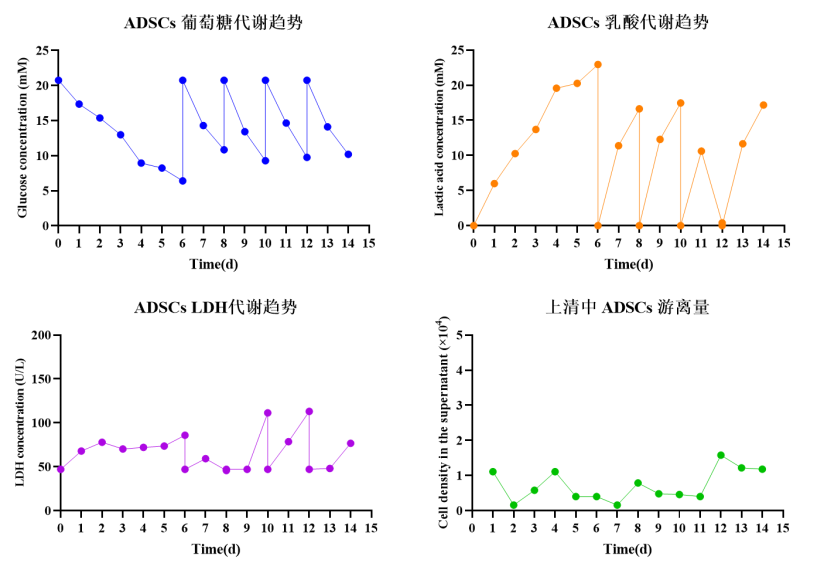
图6. ADSCs在Ad60 FBR FB-2上培养过程的生化指标

图7. ADSCs在Ad60 FBR FB-2中培养时取样条上的活细胞荧光染色情况
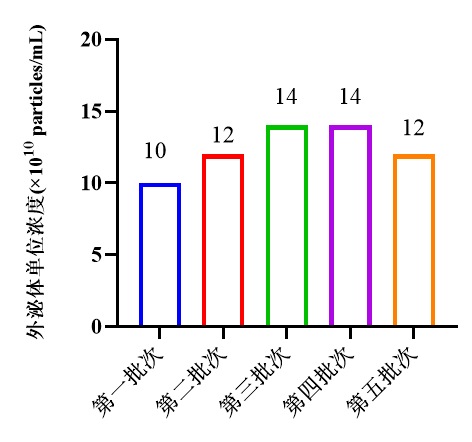
图8. ADSCs在Ad60 FBR FB-2培养收获上清中外泌体NTA检测结果
结果显示,ADSCs使用Ad60 FBR FB-2进行3D培养时,葡萄糖、乳酸、LDH等代谢参数稳定且脱落的游离细胞少。通过荧光染色观察,取样条上的细胞活率高。最终我们共收获了5批次外泌体上清原液,每批次收获颗粒浓度为10~14×1010 particles/mL,产量稳定。
ADSCs在2D培养条件下,使用不同培养基进行培养后显示使用MSC ExoPro SFM及MSC Basal SFM两款培养基细胞生长更快且外泌体产量更高(图9)。

图9. CEL-G® Culture MSC 系列完全培养基套装
ADSCs在Ad60 FBR FB-2上培养14天,最终收获外泌体总体积5.5L,每批次收获的外泌体颗粒浓度稳定达到1×1011particles/mL以上,得到外泌体总产量为6.7×1014 particles,且根据其代谢和细胞活率数据,推测具有继续收获更多批次的潜力。本次研究外泌体产量得到喜人的结果,为后续ADSCs细胞进行更大规模的培养及外泌体收获提供了可靠的数据支撑,助力深入开展ADSCs-EXOs的临床应用研究。
[1] 陈自强,米日班买买提明,李红建. 脂肪干细胞源性外泌体的应用进展[J]. 实用心脑肺血管病杂志,2023,31(2):125-129.
[2] Yang, An,Shuyan, Lin,Xiaojie, Tan et al. Exosomes from adipose-derived stem cells and application to skin wound healing.[J] .Cell Prolif, 2021, 54 (3):e12993.
[3] Reka Agnes, Haraszti,Rachael, Miller,Matteo, Stoppato et al. Exosomes Produced from 3D Cultures of MSCs by Tangential Flow Filtration Show Higher Yield and Improved Activity.[J] .Mol Ther, 2018, 26 (12):2838-2847.
- 021-50826962
- sales@ttbiotech.com
-
江苏省苏州市太仓市昭溪路90号
