-
新闻
CEL-G®TFF Lab外泌体浓缩系统:引领NK外泌体应用新纪元
发布日期:2024-12-06
在生命科学日新月异的今天,外泌体(Exosomes)作为细胞间通讯的重要载体,正逐渐成为生物医学研究和临床应用的热点。其中,自然杀伤细胞(Natural killer cell,NK细胞)外泌体以其独特的抗肿瘤、免疫调节功能,吸引了广泛关注。同腾新创自主研发的CEL-G® TFF Lab系列外泌体浓缩系统,凭借其高效、精准、自动化的特点,为NK外泌体的提取和应用提供了强有力的技术支持。本文将详细介绍NK外泌体的作用机制及TFF Lab外泌体浓缩系统在NK外泌体处理中的应用。
NK细胞作为人体免疫系统的重要组成部分,以其强大的抗肿瘤和抗病毒能力著称。近年来,科学家们发现,NK细胞不仅通过直接杀伤机制对抗肿瘤,还能通过释放外泌体来传递信息、调节免疫反应。这些外泌体富含多种生物活性分子,如蛋白质、脂质和核酸,能够参与细胞间的通讯,影响周围细胞的功能,从而在抗肿瘤、免疫调节等方面发挥重要作用。
NK细胞外泌体是NK细胞分泌的小囊泡,具有典型的磷脂双层膜结构,直径约为30-150nm。这些外泌体富含多种生物活性分子,包括蛋白质、脂质、RNA(如miRNA、mRNA)等,能够在细胞间传递信息并调节细胞功能。NK细胞外泌体不仅继承了NK细胞的抗肿瘤特性,还具备跨越物理屏障、靶向特定细胞的能力,成为肿瘤免疫治疗的新策略。
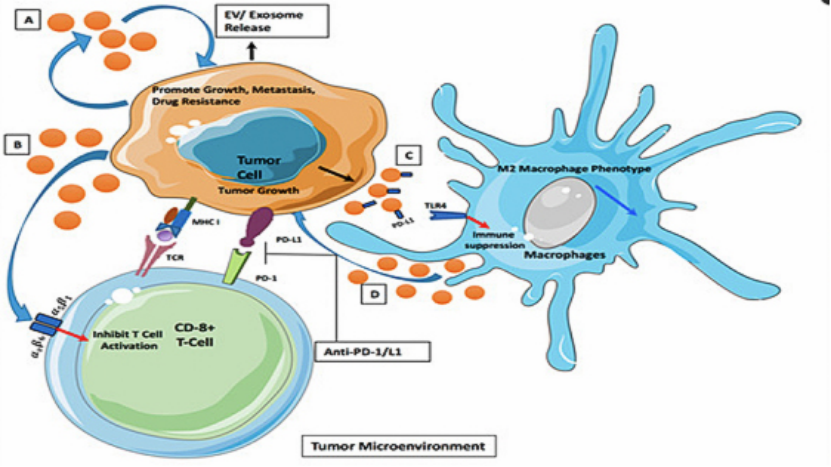
图1. NK细胞分泌的外泌体可引起肿瘤凋亡[1]
NK细胞外泌体在肿瘤治疗中的应用
2.1 抗肿瘤作用机制
NK细胞外泌体通过多种机制发挥抗肿瘤作用:
直接杀伤:外泌体中的穿孔素、颗粒酶等细胞毒颗粒可诱导肿瘤细胞凋亡。
免疫调节:外泌体中的细胞因子和趋化因子可募集并激活其他免疫细胞,共同发挥抗肿瘤作用。
药物递送:外泌体可作为抗肿瘤药物的载体,实现药物的精准递送,提高治疗效果。
2.2 临床应用案例
多项研究表明,NK细胞外泌体在体外和体内实验中均表现出显著的抗肿瘤效果。例如,韩国庆北国立大学医学院的研究发现,NK细胞外泌体对黑色素瘤细胞具有细胞毒性,并在小鼠模型中显著抑制肿瘤生长[2]。此外,通过工程化改造NK细胞外泌体,如加载特定miRNA或药物,可进一步增强其抗肿瘤效果[3]。

NK细胞外泌体在糖尿病治疗中也展现出潜在的应用价值。研究表明,来自瘦小鼠的NK细胞外泌体能够减轻肥胖诱导的Ⅱ型糖尿病小鼠模型中的胰岛素抵抗和炎症[4]。这些外泌体通过调节胰岛素信号通路和抑制炎症反应,显著改善糖尿病小鼠的胰岛素敏感性。此外,外泌体在促进糖尿病伤口愈合方面也表现出积极作用,通过调节血管生成、胶原合成和炎症抑制等过程,加速伤口愈合进程[5]。
除了肿瘤和糖尿病外,NK细胞外泌体还在皮肤病、神经退行性疾病等领域展现出潜在的治疗价值。例如,在特应性皮炎(Atopic dermatitis, AD)的治疗中,NK细胞通过调节免疫反应发挥关键作用。研究发现,AD患者血液中NK细胞数量减少,而通过增强NK细胞活性的治疗可显著改善疾病症状[6]。
NK细胞作为人体免疫系统的重要组成部分,以其强大的抗肿瘤和抗病毒能力著称。近年来,科学家们发现,NK细胞不仅通过直接杀伤机制对抗肿瘤,还能通过释放外泌体来传递信息、调节免疫反应。这些外泌体富含多种生物活性分子,如蛋白质、脂质和核酸,能够参与细胞间的通讯,影响周围细胞的功能,从而在抗肿瘤、免疫调节等方面发挥重要作用。
同腾新创自成立以来,始终站在科技前沿,不断探索与突破。CEL-G® TFF Lab系列外泌体浓缩系统,作为公司精心打造的一款高性能设备,已经在市场上赢得了广泛的认可与好评。CEL-G® TFF Lab外泌体浓缩系统,是一款基于多级分离原理实现外泌体浓缩收获的自动化处理设备。该系统采用高效的切向流过滤(Tangential Flow Filtration,TFF)技术,与传统的死端过滤不同,TFF系统的过滤液以平行于膜表面的方向流动,有效减少了膜表面的浓差极化现象,提高了过滤效率和膜的使用寿命。本系统配备控制器主机,人机交互界面和一次性封装耗材包,可实现自动运行清洗-浓缩-收获多级程序,实时监测、定量收获、高倍浓缩外泌体,耗时短、效率高,整个处理过程静音、安全、顺畅,收获的外泌体符合相关鉴定标准。

图2. CEL-G® TFF Lab系列外泌体浓缩系统
-
高效性:系统能够在不损失目标产物活性的前提下,快速完成缓冲液的替换和样品的浓缩,提高了实验效率和结果的可重复性。
-
精准性:通过精细调节操作参数(如流速、压力和缓冲液浓度),可以实现对浓缩/置换过程的精确控制,满足不同实验需求。
-
自动化:系统配备控制器主机、人机交互界面和一次性封装耗材包,自动运行清洗-浓缩-收获-缓冲液置换等多级程序,减少了人为操作带来的误差和风险。
-
灵活性:兼容多种类型的膜材料和孔径,适用于不同分子量的物质分离和纯化。
-
可扩展性:从小型实验室设备到大型工业化生产设备,TFF技术展现出良好的适应性和可扩展性。
使用CEL-G® TFF Lab系列外泌体浓缩系统高效处理9.7L NK细胞上清液收获370mL外泌体终产物,以下是NK细胞外泌体的鉴定结果:
① 纳米颗粒跟踪分析仪(NTA)检测外泌体粒子浓度及粒径范围:
经过NTA检测NK原液上清颗粒浓度为4.35×108Particles/mL,浓缩后外泌体颗粒浓度为1.65×109Particles/mL,粒径<150nm,存在峰值,经浓缩处理后粒径分布由双峰变为单峰。
表1. NTA检测NK细胞上清原液及外泌体颗粒粒径及浓度

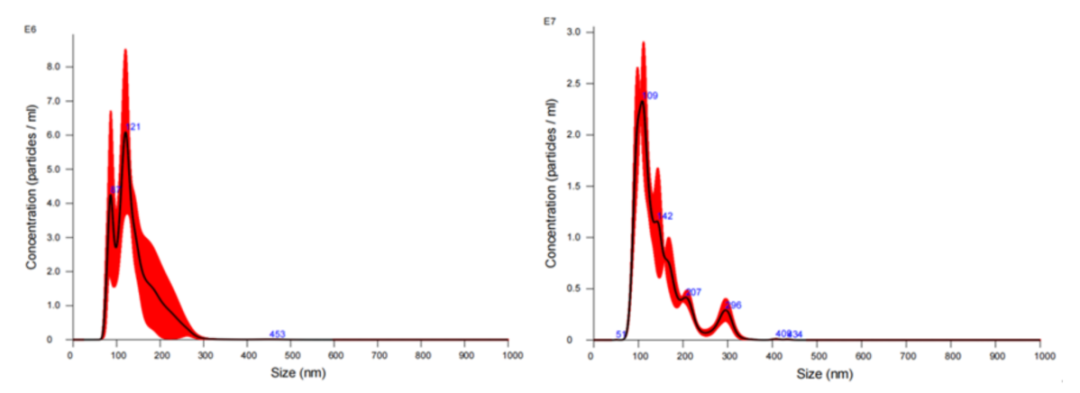
图3 NK上清原液(左)与TFF Lab 处理后NK外泌体(右)粒径分布图对比
② 免疫印迹(WB)检测外泌体表面标志物表达:
外泌体阳性表面标志物ALIX、TSG101、CD81有清晰条带,外泌体阴性表面标志物Calnexin无表达。浓缩液对比原液阳性表面标志物条带更清晰。
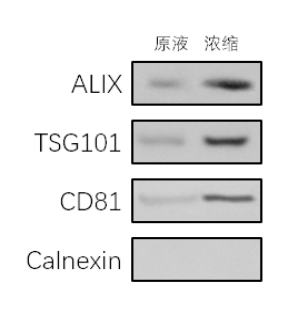
图3 WB检测NK外泌体表面标志物表达
通过以上外泌体鉴定结果表明CEL-G®TFF Lab系列外泌体浓缩系统能够从NK细胞培养上清中提取高质量外泌体,同时,处理10L NK细胞上清液仅需1h工艺处理时间,相比超速离心等传统外泌体提取方式,TFF Lab外泌体浓缩系统显著提高了外泌体提取效率,缩短了工艺处理时间的同时保持了外泌体的完整性和生物学活性。
同腾新创自主研发的CEL-G® TFF Lab系列外泌体浓缩系统,凭借其高效、精准、自动化的特点,为NK细胞外泌体的提取和应用提供了强有力的技术支持。随着研究的不断深入和技术的不断完善,NK细胞外泌体有望在癌症治疗、免疫调节和组织再生等领域发挥更大的作用。我们期待未来能够见证更多关于NK细胞外泌体的研究成果和应用案例,共同推动生物医学领域的发展和创新。
[1]Aarsund M, Nyman TA, Stensland ME, Wu Y, Inngjerdingen M. Isolation of a cytolytic subpopulation of extracellular vesicles derived from NK cells containing NKG7 and cytolytic proteins. Front Immunol. 2022 Sep 15;13:977353. doi: 10.3389/fimmu.2022.977353. PMID: 36189227; PMCID: PMC9520454.
[2]Zhu, L., et al. (2017). "Exosomes Derived From Natural Killer Cells Exert Therapeutic Effect in Melanoma." Theranostics 7(10): 2732-2745.
[3]Jong, A. Y., et al. (2017). "Large-scale isolation and cytotoxicity of extracellular vesicles derived from activated human natural killer cells." J Extracell Vesicles 6(1): 1294368.
[4]Wang, Y., Li, M., Chen, L. et al. Natural killer cell-derived exosomal miR-1249-3p attenuates insulin resistance and inflammation in mouse models of type 2 diabetes. Sig Transduct Target Ther 6, 409 (2021).
[5]Li D, Wu N. Mechanism and application of exosomes in the wound healing process in diabetes mellitus. Diabetes Res Clin Pract. 2022 May;187:109882.
[6]Mack MR, Brestoff JR, Berrien-Elliott MM, et al. Blood natural killer cell deficiency reveals an immunotherapy strategy for atopic dermatitis. Sci Transl Med. 2020 Feb 26;12(532).
- 021-50826962
- sales@ttbiotech.com
-
江苏省苏州市太仓市昭溪路90号
